灯塔水母的细胞逆转机制:技术极客视角下的生物学突破
2019年深秋,我第一次在显微镜下观察到灯塔水母的细胞转分化过程。那一刻,实验室的寂静被某种难以名状的震撼打破——一个直径仅4~5毫米的透明生物体,正在上演生命科学领域最不可思议的逆转剧。
理论框架与技术背景
灯塔水母(Turritopsisnutricula)属于水螅纲棒螅水母科,其核心生存机制建立在细胞全能性的递归应用之上。与哺乳动物细胞高度分化的特性不同,灯塔水母的体细胞保留了类似干细胞的去分化潜能。这种生物学特性使得该物种在面临环境胁迫时,能够启动独特的逆向发育程序。
从发育生物学角度分析,灯塔水母的生命周期包含两个主要阶段:营固着生活的螅状体阶段和自由漂浮的成体水母阶段。传统水母的发育路径是单向不可逆的,而灯塔水母则实现了阶段间的双向转换。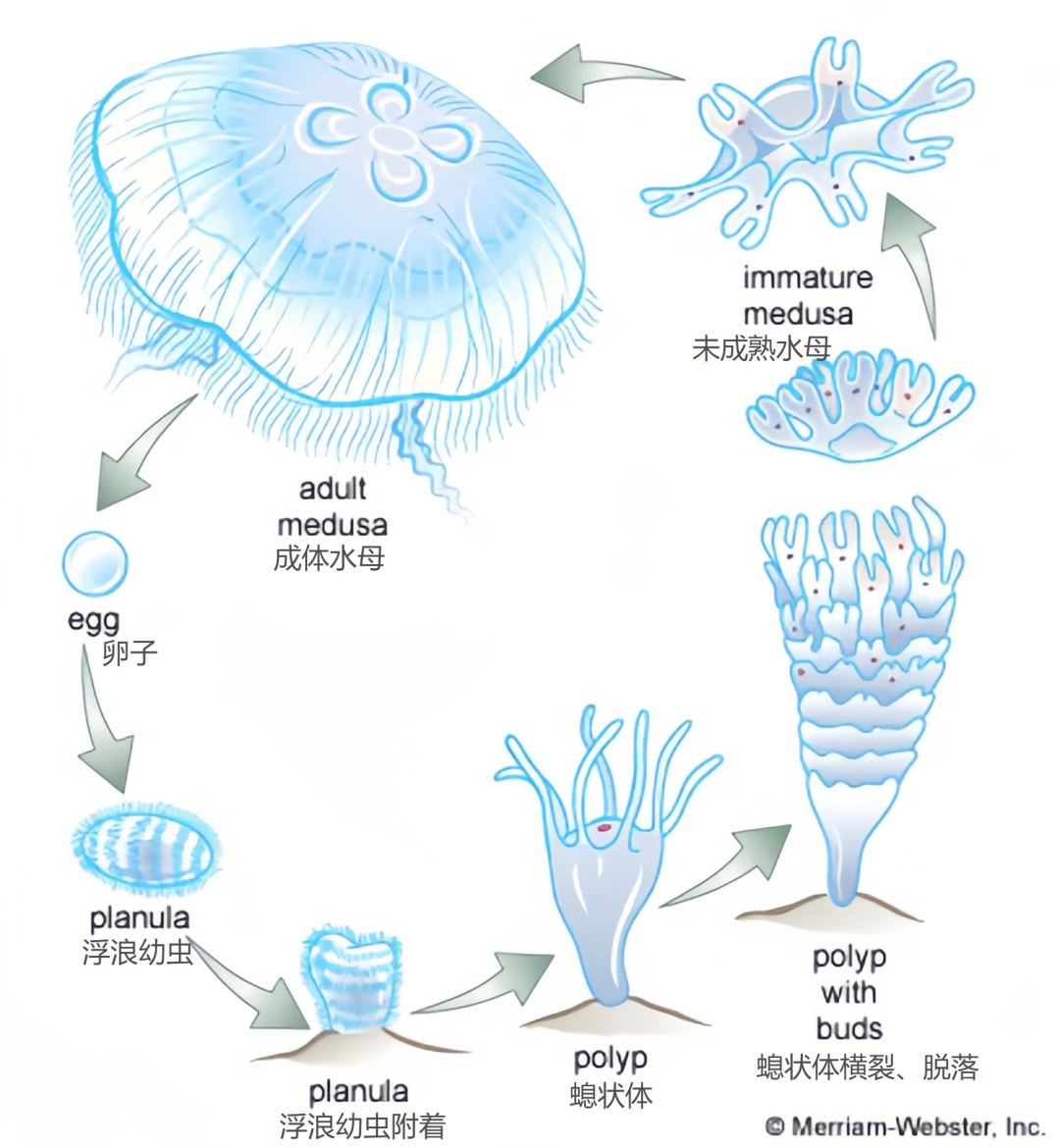
细胞转分化的分子机制
当灯塔水母遭受物理损伤或营养胁迫时,其触手动膜细胞率先启动去分化程序。这些高度特化的细胞通过表观遗传重塑,回归到类似多能干细胞的状态,形成胞囊结构。该过程中,细胞特异性基因被沉默,而发育调控基因(如Wnt、Notch家族成员)被重新激活。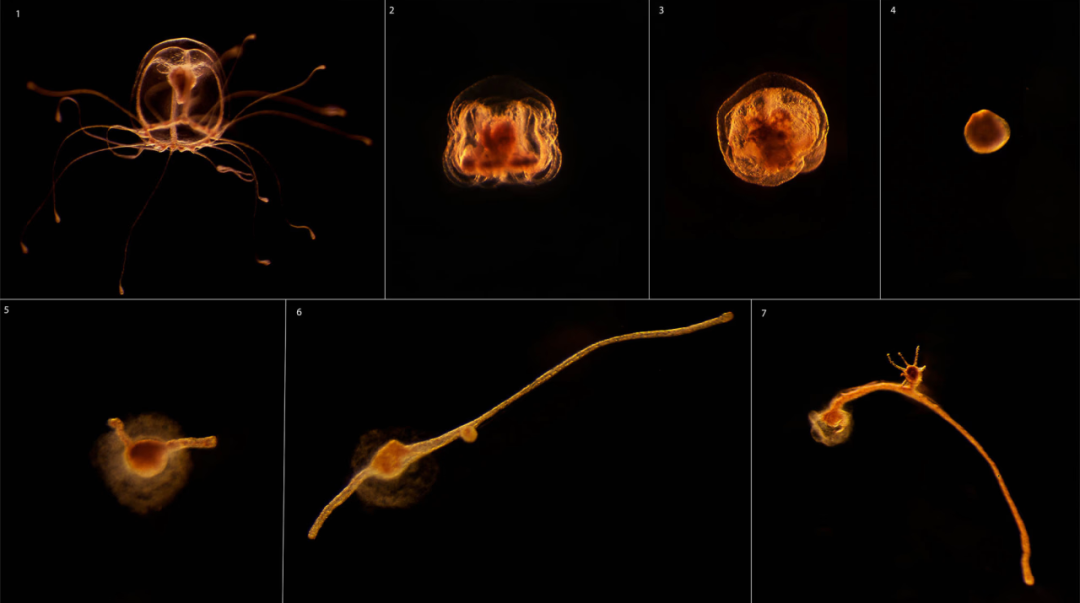
胞囊在海底沉降后的24~36小时内完成形态重构。新的螅状体由胞囊细胞经选择性基因表达分化而来,其体壁细胞、消化细胞、刺细胞依次形成。这一过程的能量消耗与物质基础,正是灯塔水母长期演化的结果。
实验数据与寿命推演
日本生物学家久保田拓自1990年代起的长期观察记录显示,在可控实验室环境中,灯塔水母可在两年观察期内完成至少10次完整的生命周期转换。这意味着该物种的时间尺度远超人类直觉理解——其生命周期可压缩至一个月级别。
然而必须指出,灯塔水母的永生具有严格的边界条件:被天敌捕食、病原体感染或物理环境剧变均会导致生命终结。换言之,永生仅存在于理想化的生物学模型中。
技术转化路径与局限
目前科学界对灯塔水母机制的研究聚焦于两个方向:一是解析去分化过程中关键转录因子的调控网络,二是探索如何在哺乳动物细胞中重建类似的细胞可塑性。尽管诱导性多能干细胞(iPSC)技术已部分实现细胞命运的逆向调控,但要在组织或器官层面复现灯塔水母的全身性更新,仍面临巨大的技术障碍。
对于生命科学领域的研究者而言,灯塔水母的启示在于:细胞命运的plasticity远比传统认知更具弹性。这一发现为再生医学、衰老干预等领域提供了新的研究范式。
